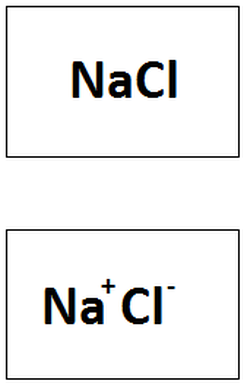Enlaces Químicos
Un enlace químico corresponde a la fuerza que une o enlaza a dos átomos, sean estos iguales o distintos. Los enlaces se pueden clasificar en tres grupos principales: enlaces iónicos, enlaces covalentes y enlaces dativos. Los enlaces se producen como resultado de los movimientos de los electrones de los átomos, sin importar el tipo de enlace que se forme. Pero no cualquier electrón, puede formar un enlace, sino solamente los electrones del último nivel energético (más externo). A estos se les llama electrones de valencia. En este capítulo analizaremos las características de cada tipo de enlace, como también veremos diferentes maneras de representarlos en el papel. Partiremos definiendo lo que es un enlace iónico.
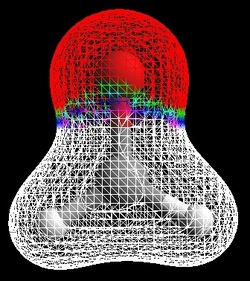
Imagen 27: Vista 3D de la Molécula de NaCl (sal de mesa).
- Enlace iónico: Un enlace iónico se puede definir como la fuerza que une a dos átomos a través de una cesión electrónica. Una cesión electrónica se da cuando un elemento electropositivo se une con un elemento electronegativo. Mientras mayor sea la diferencia de electronegatividad entre los elementos, más fuerte será el enlace iónico. Se empieza a considerar que dos átomos están unidos a través de un enlace iónico cuando su diferencia de electronegatividad es superior a 1.7. Un ejemplo de un compuesto unido a través de enlace iónico se muestra en la Imagen 27, mientras que en laImagen 28 se ve algunas maneras de escribir compuestos unidos mediante este tipo de enlace.
Imagen 27: Vista 3D de la Molécula de NaCl (sal de mesa).
Imagen 28: Formas de escribir una molécula que está unida mediante un enlace Iónico.
- Enlace Covalente: El enlace covalente es la fuerza que une dos átomos mediante la compartición de un electrón por átomo. Dentro de este tipo de enlace podemos encontrar dos tipos: el enlace covalente polar y el enlace covalente apolar. El primer sub-tipo corresponde a todos aquellos compuestos en donde la diferencia de electronegatividad de los átomos que lo componen va desde 0 hasta 1.7 (sin considerar el 0). Los compuestos que son polares se caracterizan por ser asimétricos, tener un momento dipolar (el momento dipolar es un factor que indica hacia donde se concentra la mayor densidad electrónica) distinto a 0, son solubles en agua y otros solventes polares, entre otras características. Dos ejemplos se ven en laImagen 29 (a) y en la Imagen 29 (b), respectivamente. Por su parte, los compuestos que se forman por medio de enlaces covalentes apolares, no presentan momento dipolar, la diferencia de electronegatividad es igual a 0, son simétricos, son solubles en solventes apolares (como el hexano), entre otras cosas. La diferencia de electronegatividad cero se da cuando dos átomos iguales se unen entre sí, como por ejemplo la molécula de Nitrógeno o la molécula de Cloro (ver Imagen 30 (a) e Imagen 30 (b) respectivamente).
Imagen 29: Densidades electrónicas en los siguientes compuestos polares: a) formaldehído (o metanal); b) 1,2-difluoretano. El color blanco indica una escasez de electrones, de ahí vienen respectivamente el color violeta, azul, verde y rojo (el cual indica mayor densidad electrónica).
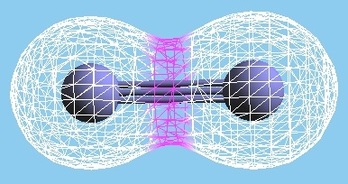
Imagen 30: Densidades electrónicas en a) la molécula de Nitrógeno; b) la molécula de Cloro. El color blanco denota una escasez electrónica mientras que lo más violeta indica una zona más rica en electrones.
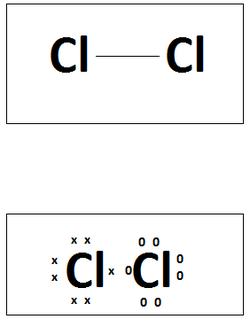
En la Imagen 31 se puede ver formas de escribir un enlace covalente. La imagen superior corresponde a lo que se llama estructuras de Kekulé, mientras que la inferior se denomina estructuras de Lewis. Se profundizará algo más esto cuando veamos ácido-base.
Imagen 31: Formas de dibujar un enlace covalente en el papel.
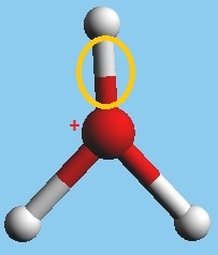
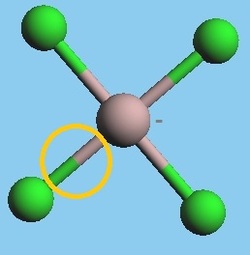
- Enlace Covalente Coordinado o Dativo: Si bien se clasifica también como enlace covalente, algunos químicos difieren de llamarlo así debido a que, como se dijo anteriormente, en un enlace covalente, los dos átomos que forman dicho enlace aportan un electrón cada uno, es por eso que se le coloca por separado. Este tipo de enlace se caracteriza porque el par electrónico del enlace es entregado por un sólo átomo, el cual debe poseer a lo menos un par de electrones libres sin enlazar (Como el Oxígeno, Nitrógeno o Cloro, por ejemplo). Otra característica importante es que el átomo que acepta el par electrónico debe estar carente de electrones (como el ión hidrógeno [más conocido como protón], el Aluminio, entre otros). Este tipo de enlace es muy importante para el capítulo de ácidos-bases (que se verá a continuación) debido a que una teoría ácido-base indica que un ácido es aquella sustancia química que es capaz de aceptar un par electrónico y una base una sustancia capaz de compartirlos. También los enlaces dativos sirven para poder comprender de mejor manera la disolución de sustancias (tema que se verá más adelante). En la Imagen 32 (a) y en la Imagen 32 (b) se pueden ver dos ejemplos de sustancias con un enlace dativo.
Imagen 32: Sustancias que contienen un enlace dativo (encerrado en el círculo naranja): a) ión hidronio; b) ión tetracloruro de Aluminio.
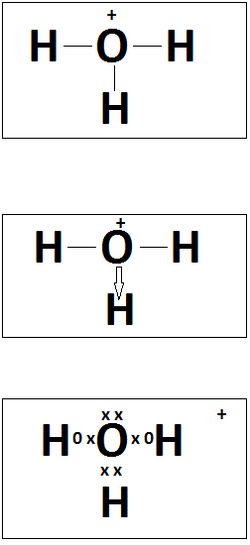
En la Imagen 33 se ven tres formas de escribir un enlace dativo, en este caso se usó de ejemplo el ión hidronio. Por lo general se suele utilizar la estructura de Kekulé normal (superior), aunque muchos prefieren usar esa especie de estructura de Kekulé modificada (centro), ya que denota la presencia de un enlace con carácter distinto (en la imagen superior se podría pensar que los 3 enlaces son de la misma naturaleza). La estructura de Lewis (inferior) es poco usual, aun así es muy útil para ver comportamientos de solubilidad o ácido-base.
Imagen 33: Formas de escribir un enlace covalente coordinado en el papel.
Con esto terminamos lo relacionado a enlaces químicos y tenemos las herramientas suficientes para empezar a comprender mejor como funciona una reacción ácido-base. Pero antes de eso, es necesario tener claro lo que es una disolución y cuáles son sus unidades de medición.